“Zastosowanie sztucznej inteligencji do przewidywania obecności skrzepliny w uszku lewego przedsionka w oparciu o obraz video echokardiografii przezklatkowej oraz dane kliniczne.”
Numer projektu:
UMO-2023/51/D/NZ5/02583

1. Wprowadzenie:
Migotanie przedsionków (AF) stanowi krytyczne obciążenie dla współczesnych systemów ochrony zdrowia, dotykając szacunkowo 37% populacji europejskiej powyżej 55. roku życia. Z perspektywy klinicznej, kluczowym zagrożeniem wynikającym z AF nie jest sama arytmia, lecz jej profil hemodynamiczny sprzyjający powstawaniu skrzeplin (LAT) – najczęściej w uszku lewego przedsionka (LAA). Ich embolizacja do krążenia mózgowego jest bezpośrednią przyczyną udarów niedokrwiennych.
Identyfikacja obecności LAT jest punktem zwrotnym w procesie decyzyjnym kardiologa. Procedury takie jak kardiowersja elektryczna czy ablacja przezskórna mogłyby stanowić zagrożenie dla zdrowia pacjenta w przypadku obecności skrzepliny, gdyż mogą wywołać jej oderwanie. Dlatego precyzyjne wykluczenie LAT jest niezbędne dla bezpieczeństwa pacjenta i skutecznego planowania leczenia. Obecnie, mimo stosowania doustnej antykoagulacji, ryzyko formowania się skrzeplin nie zostaje całkowicie wyeliminowane, co potęguje zapotrzebowanie na wiarygodną diagnostykę obrazową.
2. Paradygmat diagnostyczny:
Obecny standard diagnostyczny opiera się na napięciu między wysoką czułością, a inwazyjnością badań. Chociaż echokardiografia przezprzełykowa (TEE) pozostaje „złotym standardem”, jej ograniczenia definiują istotną, niezaspokojoną potrzebę kliniczną (unmet clinical need).
Ograniczenia metody TEE:
- Wysoka inwazyjność: Konieczność wprowadzenia sondy przez przełyk wywołuje znaczny dyskomfort i stres u pacjenta.
- Ryzyko powikłań: Możliwość urazów mechanicznych górnego odcinka układu pokarmowego i krtani.
- Logistyka i zasoby: Badanie jest czasochłonne, wymaga specjalistycznego przygotowania pacjenta oraz rygorystycznej sterylizacji sprzętu.
- Zmienność interpretacyjna: Wynik badania w dużym stopniu zależy od doświadczenia operatora.
Alternatywą jest echokardiografia przezklatkowa (TTE) – metoda szybka i nieinwazyjna. Choć TTE nie pozwala na bezpośrednie uwidocznienie uszka lewego przedsionka, dostarcza szeregu parametrów hemodynamicznych korelujących z ryzykiem zakrzepowym. Wyzwaniem jest stworzenie modelu, który pozwoli TTE na dostarczanie danych o ryzyku LAT z precyzją zbliżoną do badania przezprzełykowego.
3. Architektura rozwiązania:
Aby wyeliminować ograniczenia dotychczasowych modeli, które wymagały ręcznego wprowadzania licznych parametrów , wdrożyliśmy w pełni zautomatyzowany system analizy nagrań wideo z echokardiografii przezklatkowej (TTE) oparty na głębokich sieciach konwolucyjnych. Zastosowanie tego rozwiązania pozwala na eliminację błędów wynikających ze zmienności międzyobserwacyjnej, znacząco poprawiając powtarzalność wyników. Ponadto, sztuczna inteligencja umożliwia ekstrakcję ukrytych cech hemodynamicznych, takich jak prędkość przepływu w uszku lewego przedsionka (LAAV), których nie można tradycyjnie zmierzyć w badaniu TTE.
Krok 1: Ekstrakcja cech i automatyczna segmentacja
Wykorzystując referencyjny zbiór danych EchoNet, zawierający 10 030 nagrań z echokardiografii przezklatkowej (TTE), model sztucznej inteligencji oparty na architekturze U-Net lub Echonet-Dynamic dokonuje automatycznej segmentacji lewego przedsionka (LA) i lewej komory (LV). Pozwala to na wygenerowanie krzywych pola powierzchni w czasie (area-time curves) , które precyzyjnie opisują rozmiar i funkcję jam serca.
Krok 2: Predykcja LAT i modelowanie LAAV
W drugim etapie model integruje wygenerowane przez AI dane obrazowe z kontekstem klinicznym, obejmującym choroby współistniejące oraz farmakoterapię. Istotnym elementem projektu jest wykorzystanie uczenia maszynowego do jednoczesnej predykcji obecności skrzepliny (modele klasyfikacyjne) oraz szacowania prędkości przepływu w uszku lewego przedsionka (LAAV – modele regresyjne). LAAV jest kluczowym, ilościowym parametrem zastępczym (surogatem) ryzyka zakrzepowo-zatorowego , którego obecnie nie można zmierzyć lub oszacować za pomocą standardowego badania TTE i który dotychczas wymagał przeprowadzenia bardziej inwazyjnego badania przezprzełykowego (TEE).
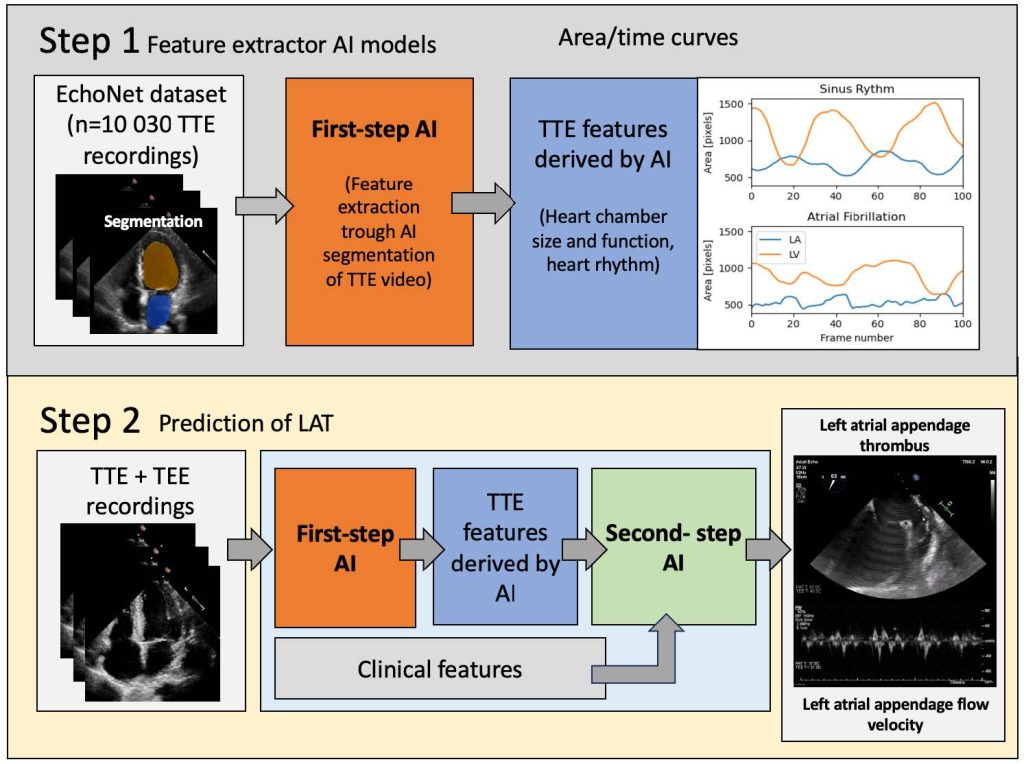
Automatyzacja eliminuje konieczność ręcznego wprowadzania 39 parametrów klinicznych, skracając czas analizy do sekund i zapewniając pełną powtarzalność wyników.
4. Dowody naukowe i potencjał wdrożeniowy (Rejestr LATTEE):
Podstawą projektu są wyniki wieloośrodkowego rejestru LATTEE (N=4302), które zostały nagrodzone podczas Kongresu ESC 2022 i opublikowane w „European Heart Journal”. Wstępne badania dowiodły, że model wykorzystujący parametry TTE osiąga wysoką zdolność dyskryminacyjną.
Kluczowe wskaźniki naukowe:
- Skuteczność: Model osiągnął wskaźnik AUC na poziomie 0.85 w przewidywaniu skrzeplin.
- Bezpieczeństwo kliniczne: Przy optymalizacji punktu odcięcia, model wykazał 99% ujemną wartość predykcyjną (NPV). Oznacza to, że narzędzie bezbłędnie identyfikuje pacjentów wolnych od skrzeplin.
- Optymalizacja systemowa: Zastosowanie tego algorytmu pozwoliłoby uniknąć 40% inwazyjnych badań TEE u pacjentów skutecznie leczonych przeciwkrzepliwie, nie pomijając przy tym żadnej skrzepliny.
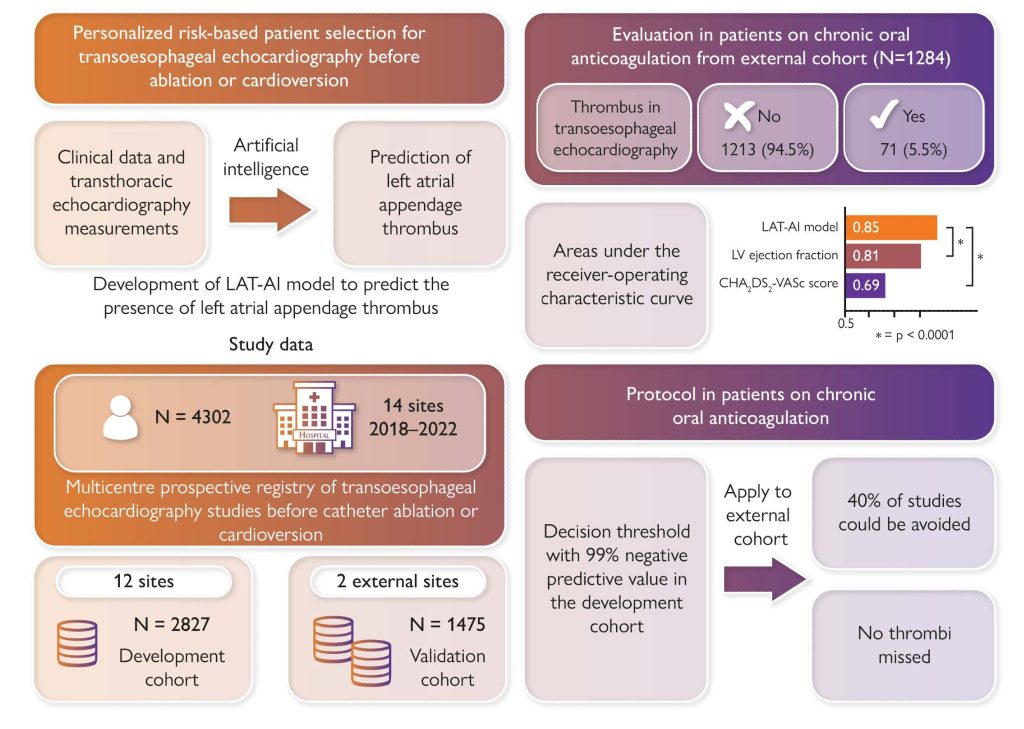
Obecne prace w ramach grantu SONATA mają na celu zastąpienie manualnych pomiarów, na których opierały się powyższe wyniki, w pełni autonomiczną analizą wideo-to-prediction, co jeszcze bardziej podniesie precyzję i użyteczność kliniczną narzędzia.
5. Podsumowanie:
Rozwijany model AI stanowi paradygmatyczną zmianę w kardiologii – przejście od medycyny reaktywnej do predykcyjnej i spersonalizowanej. Projekt opiera się na trzech filarach korzyści:
- Komfort pacjenta: Radykalne ograniczenie liczby procedur półinwazyjnych (TEE) na rzecz bezpiecznej diagnostyki przezklatkowej.
- Efektywność ekonomiczna: Optymalizacja kosztów poprzez precyzyjną selekcję pacjentów do badań inwazyjnych i skrócenie ścieżki diagnostycznej.
- Wsparcie decyzji klinicznych: Dostarczenie lekarzowi obiektywnego, ilościowego narzędzia do oceny ryzyka zakrzepowego (LAT i LAAV).
Sztuczna inteligencja, działając jako zaawansowany ekstraktor cech hemodynamicznych, staje się kluczowym partnerem kardiologa w walce z powikłaniami migotania przedsionków.


